La start-up française Diabeloop injecte de l’IA dans le quotidien des diabétiques
⏱ 5 minDepuis ce mois d’octobre, certains diabétiques peuvent bénéficier en France d’un dispositif développé par la start-up Diabeloop faisant appel à l’IA pour automatiser la délivrance de l’insuline.
De la découverte de l’insuline dans un petit laboratoire de Toronto (Canada) à la gestion automatisée de son injection grâce au machine learning, il se sera écoulé… 100 ans. L’insuline est une hormone vitale, produite par le pancréas de façon continue pour réguler la glycémie, le taux de sucre dans le sang. Sa sécrétion est sans cesse adaptée aux besoins, selon les aliments que nous mangeons, notre activité physique, notre stress, etc. Mais elle est en revanche défaillante chez les diabétiques, qui représentent au moins 5% de la population française. Le diabète reste une maladie grave, qui tue 35 000 personnes chaque année en France, 1.5 million dans le monde.
La grande majorité (près de 90%) des diabétiques souffrent d’une mauvaise utilisation de l’insuline par leur organisme, qui peut induire une baisse de sa production par le pancréas : c’est le diabète de type 2, une pathologie évolutive, souvent asymptomatique au début, sous-diagnostiquée, qui se déclare en général au-delà de la quarantaine. Un régime et des médicaments antidiabétiques permettent souvent de le maîtriser, mais il peut s’aggraver au point de nécessiter des injections d’insuline.
A contrario, le diabète de type 1 qui concerne environ 10% des cas, 250 000 en France, se découvre chez des patients jeunes, parfois dès la petite enfance. C’est une maladie auto-immune : le pancréas ne sécrète plus d’insuline car il est détruit par le système immunitaire de ces patients. Lesquels mourraient en quelques années il y a un siècle. De nos jours ils survivent grâce à des injections d’insuline au quotidien et à vie.
Le délicat apprentissage de l’équilibrage insuline/glycémie
« Notre métier est d’apprendre au patient à calculer ses doses d’insuline en fonction de ce qu’il mange, de son activité et de sa glycémie, rappelle Guillaume Charpentier, ancien chef du département diabète et endocrinologie du Centre Hospitalier Sud Francilien, à Corbeil-Essonnes. Ce qui suppose aussi de mesurer son taux de glycémie plusieurs fois par jour. Un fardeau épouvantable à gérer au quotidien ! » La disponibilité croissante de données et les progrès du machine learning ont ouvert la voie pour remplacer cet apprentissage du patient par de l’apprentissage automatique.
Mais avant de parler d’intelligence artificielle, reprenons le fil de l’histoire. Progressivement, des systèmes d’injection d’insuline de plus en plus efficaces et pratiques ont été développés. Depuis 20 ans, la plupart des patients utilisent des « stylos à insuline », rechargeables ou à usage unique, ce qui permet des injections plus simples qu’avec une seringue, mais qui restent fastidieuses puisqu’elles doivent être renouvelées plusieurs fois par jour pour les diabétiques de type 1, notamment avant chaque repas. Désormais, certains se tournent vers des pompes à insuline qui la délivrent en continu via un cathéter sous la peau, mais il leur faut toujours mesurer leur taux de glycémie plusieurs fois par jour et activer en conséquence l’injection d’insuline.
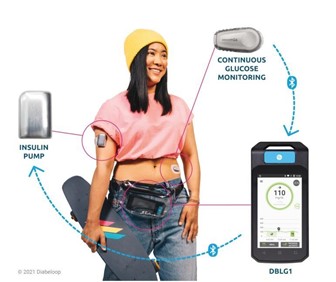
Capteur de glucose et pompe à insuline communiquent en Bluetooth avec un terminal dédié : les nouveaux systèmes automatisés (ici le DBLG1 de Diabeloop) sont désormais capables de gérer les injections d’insuline en continu. ©Diabeloop.
L’avènement de l’apprentissage automatique
Dernière nouveauté : asservir ces injections via des algorithmes d’apprentissage automatique à une mesure du glucose fournie toutes les cinq minutes par un capteur sous-cutané. Depuis quelques mois, une start-up française, Diabeloop, propose un tel système de délivrance automatisée d’insuline, le DBLG1. Quelques milliers de patients en sont déjà équipés en Allemagne, Italie, Espagne, Pays-Bas et Suisse. Il est désormais disponible en France, remboursé par la Sécurité Sociale depuis ce mois d’octobre 2021 pour certains diabétiques de type 1 adultes. Deux entreprises commercialisent également de tels systèmes aux États-Unis : Medtronic et Tandem.
L’histoire de Diabeloop commence au Centre d’Etude et de Recherche pour l’Intensification du Traitement du Diabète (CERITD), un organisme dédié au diabète et créé en 2006 par les diabétologues Guillaume Charpentier et Sylvia Franc. « Nous avons travaillé avec le CEA à partir de 2011 pour développer des algorithmes sur la base de mesures physiologiques obtenues auprès de patients de notre hôpital. Et en 2015, nous avons créé Diabeloop sur fonds propres pour perfectionner et commercialiser le système », explique Guillaume Charpentier, aujourd’hui directeur médical de Diabeloop.
Depuis, la start-up a obtenu le marquage CE en novembre 2018 pour son système DBLG1, a réalisé la plus importante levée de fonds en Europe dans le secteur de l’intelligence artificielle thérapeutique (31 millions d’euros en novembre 2019), a obtenu l’autorisation de la Haute Autorité de Santé ainsi que la prise en charge par la Sécurité Sociale fin septembre dernier, et a amorcé les démarches auprès de la FDA (Food and Drug Administration) pour une commercialisation aux États-Unis.
À la différence de Medtronic et Tandem, qui sont des fabricants de matériels, Diabeloop s’est engouffré dans ce secteur d’activités en développant des algorithmes, en collaboration avec des médecins. « Notre réussite rapide repose sur l’association datascience-simulation-physiologie du diabète, explique Erik Huneker, CEO de Diabeloop qui compte une vingtaine de spécialistes des sciences des données sur 120 salariés. Le diabète est une maladie complexe sur laquelle on ne peut pas plaquer une solution générique. Nous avons conçu un modèle qui apprend la physiologie et le mode de vie de chaque diabétique. Il prend des décisions d’injection d’insuline en temps réel en associant un fonctionnement explicable, à base d’arbres de décision qui reproduisent le raisonnement du diabétologue, avec des algorithmes de machine learning, qui restent des « boîtes noires ». Nous garantissons ainsi un compromis entre sécurité et efficacité personnalisée. Pour cela, la qualité des données exploitées dans la phase d’apprentissage est cruciale : des courbes de glycémie ne suffisent pas pour qualifier un modèle, les données en open data sont inexploitables. »
Exploiter la puissance du machine learning, sous contrôle
Le système comporte plusieurs étages, encadrés par un « superviseur » qui détecte toute situation inhabituelle. Un premier module est capable d’informer le patient qu’il est en sécurité, autrement dit s’il n’a pas de risque d’hypoglycémie. Dans le cas inverse, le risque détecté peut se traduire par une alarme. « C’est un système expert qui analyse les mesures de glycémie, explique Erik Huneker. Si tout va bien, les algorithmes de machine learning font alors des prédictions de glycémie et provoquent les injections d’insuline en conséquence. Une journée de données leur suffit pour être fonctionnels : c’est un modèle hybride de machine learning faisant appel à des réseaux de neurones, à des algorithmes génétiques et au transfer learning. Ce calcul est assorti d’indices de confiance qui traduisent à quel point le modèle comprend la situation du patient. Dès que le superviseur juge que ce module en machine learning ne comprend pas suffisamment bien la situation, un système expert reprend la main, et ce de manière automatique, transparente pour le patient : il reproduit les décisions que prendrait un diabétologue. »
Plusieurs fois par jour, un autre algorithme analyse les tendances de fond du patient en fonction de sa physiologie propre et de ses réactions puis réinjecte ces tendances dans la gestion des prédictions. Cet auto-apprentissage sur le long terme est fonctionnel au bout d’une semaine. « Les prédictions sont optimales et le régime stable au bout de 4 à 6 semaines, se réjouit Erik Huneker. La seule chose que doit faire le patient est d’indiquer au système quand il mange, sans plus de précision, ou qu’il va faire du sport. Mais s’il ne le fait pas, le système est néanmoins assez robuste pour s’ajuster de façon autonome, avec un certain délai. Dans son diabète comme pour le reste… chacun gère sa vie à sa façon, en choisissant ses propres compromis. »
Les adolescents, notamment, ont du mal à se plier à cette contrainte. « Nous lançons justement un essai clinique européen en 2022 avec des adolescents pour mieux tester cette option sans déclaration des repas, précise le CEO. Par ailleurs, nous avons lancé un partenariat avec STMicroelectronics pour mieux évaluer à l’aide de capteurs certains éléments de la vie du patient comme son émotivité, qui perturbent aussi la glycémie. » De quoi réguler un peu plus précisément la glycémie des diabétiques. Et les soulager d’autant mieux.
Isabelle Bellin
Image en une : copyright ©OMS/A. Loke
Pour en savoir plus :
*** P.Y. Benhamou et al., “Closed-loop insulin delivery in adults with type 1 diabetes in real-life conditions: a 12-week multicentre, open-label randomised controlled crossover trial”. The Lancet, Digital Health, 2019. doi.org
*** C. Amadou et al., “Diabeloop DBLG1 Closed-Loop System Enables Patients With Type 1 Diabetes to Significantly Improve Their Glycemic Control in Real-Life Situations Without Serious Adverse Events: 6-Month Follow-up”. Diabetes Care, 2021. doi.org
*** C. J. Zúñiga-Aguilar et al., “Blood glucose prediction with a fractional order neural network”. Conference: Advanced Technologies & Treatments for Diabetes, 2020, doi.org








